Espaciadores autodirigidos: dilucidando las funciones no canónicas de los sistemas CRISPR
¿Qué son los sistemas CRISPR?
En los últimos años, CRISPR ha tomado gran relevancia en el ámbito de la biología gracias al enorme potencial en edición genómica mostrado por las “tijeras genéticas” CRISPR-Cas9, que fueron desarrolladas por Emmanuelle Charpentier y Jennifer A. Doudna lo que las hizo acreedoras del premio Nobel de Química en el año 2020; su trabajo publicado en el año 2012 titulado: “A programmable dual-RNA-guided DNA endonuclease in adaptive bacterial immunity” dio la vuelta al mundo y fue de gran importancia para el desarrollo de este método de edición genómica. El descubrimiento principal para la creación de esta herramienta se dio por casualidad: durante los estudios de Emmanuelle Charpentier sobre el patógeno Streptococcus pyogenes, Charpentier identificó que una molécula previamente conocida como ARNtracr era parte de los sistemas CRISPR/Cas cuya función canónica es conferir resistencia a patógenos externos como los virus, con base en esto Charpentier y Doudna recrearon las “tijeras genéticas” de las bacterias en un tubo de ensayo y revolucionaron la historia de la medicina (Alcalde 2020).
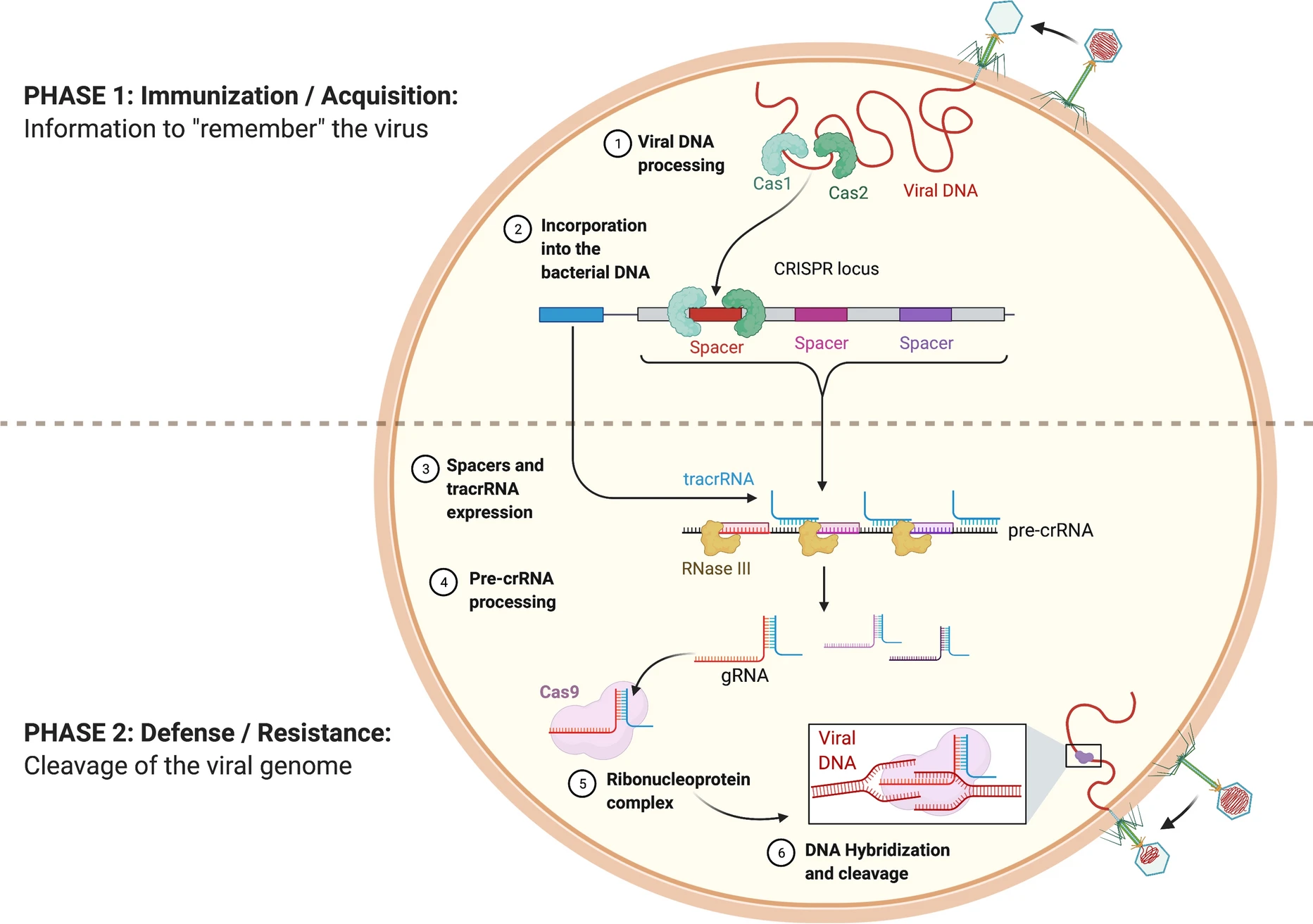
Los sistemas CRISPR/Cas funcionan como sistemas inmunes en las bacterias y arqueas; estos les permiten defenderse de virus que las han infectado previamente: ¡tienen memoria! CRISPR por sus siglas en inglés Clustered Regularly Interspaced Short Palindromic Repeats son una serie de secuencias de ADN presentes en el genoma de algunos organismos procariotas, esta serie de regiones son responsables del funcionamiento del sistema inmune que poseen estos organismos contra la integración de material genético exógeno. Este complejo sistema está formado por el operón Cas que alberga los datos genéticos necesarios para la producción de las endonucleasas Cas (CRISPR associated) junto con otras proteínas cruciales para el funcionamiento del sistema CRISPR/Cas, además de la región CRISPR que contiene repeticiones alternadas con cortas secuencias espaciadoras, las cuales son incorporadas a partir de fuentes externas durante infecciones, estos espaciadores se unen por complementariedad a la secuencia objetivo guiando así a las proteínas Cas asociadas y promoviendo la degradación del material genético exógeno.
El fenómeno del “self-targeting”
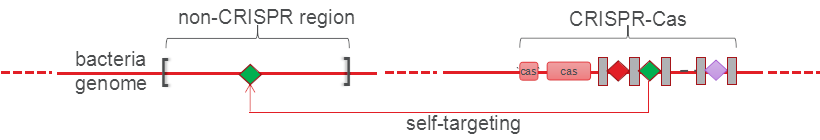
Aunque la principal función conocida de los sistemas CRISPR sea la defensa ante virus, también se han encontrado espaciadores autodirigidos (“self-targeting spacers”), es decir, que son complementarios a partes del propio genoma de la bacteria y presuntamente resultan en una autoinmunidad, esto representa una paradoja para la cual se han propuesto dos posibles soluciones: la primera es que sean “accidentes” biológicos que ocurren al azar y a los cuales la bacteria tiene que hacer frente, mientras que la segunda propone que estén relacionados con funciones no canónicas, es decir diferentes a la función inmunitaria de los sistemas CRISPR; estas funciones alternativas son un área de investigación muy poco explorada en biología que podría tener importantes implicaciones en cuanto al conocimiento de los sistemas CRISPR y el desarrollo de interesantes herramientas moleculares. (Wimmer y Beisel 2020).
El objetivo de esta línea de investigación es ahondar en el conocimiento de las funciones no canónicas de los sistemas CRISPR y ayudar a dilucidar la paradoja de los espaciadores autodirigidos mediante el uso de herramientas computacionales para el análisis de datos genómicos disponibles en línea. Te invitamos a unirte a este fascinante proyecto de investigación, en el que fusionamos diferentes áreas del conocimiento científico, ¡tu participación podría contribuir significativamente a la comprensión de estos procesos biológicos!